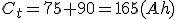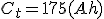La batería.

Al comienzo de la jornada laboral María y Lorenzo tienen que reparar un vehículo que no arranca.
Lorenzo le dice a María:
─Lo primero que voy a mirar es la batería, porque estoy casi seguro que eso.
─Que no se te el polímetro y ten cuidado que ya sabes que si te cae líquido de la batería en la ropa se te estropea.
─No te preocupes, estaré atento, voy a coger el polímetro y también un densímetro.
─Perfecto yo traigo el comprobador de batería y te ayudo.

1.- La batería.
María y Lorenzo comentan el arreglo de la batería y disfrutan pensando en lo que están aprendiendo en las prácticas y los problemas que tenían anteriormente a causa del mal funcionamiento de la batería de sus vehículos y que con los estudios de este capítulo en el Instituto han podido solucionar.

¿Te habías preguntado alguna vez de dónde sacamos la energía para la puesta en marcha del motor? Esta energía la sacamos de la batería.
La batería forma parte del circuito de carga y arranque, es el componente eléctrico que va a suministrar la energía necesaria en el momento de puesta en marcha del motor térmico; también es el componente que recibe la corriente eléctrica generada por el alternador y almacenándola en forma de energía química en su interior para su posterior utilización. La transformación de energía eléctrica en química se hace de forma reversible, durante un determinado número de veces, que variara en función de la calidad de los elementos que la constituyen.
Las baterías generalmente tienen una tensión de 12 voltios, aunque se pueden encontrar baterías de 6 y 24 voltios.
La elección de la batería para su uso en un automóvil está determinada por el tipo de motor y su cilindrada, también se debe tener en cuenta las condiciones climatológicas de la zona por las que circulara el vehículo, ya que la capacidad de la batería disminuye con las bajas temperaturas, pudiendo suponer un problema en el momento del arranque.
1.1.- Componentes de un acumulador de plomo.
¿Te has preguntado de qué materiales se fabrican los acumuladores?
Los acumuladores se distinguen unos de otros por el material del que están fabricados los elementos que lo componen, en este caso el material que se utiliza como sustancia activa es el peróxido de plomo (PbO2) en el ánodo, o polo positivo y plomo esponjoso (Pb) en el cátodo, o polo negativo y como electrólito una solución ácida de agua destilada (H2O) y ácido sulfúrico (H2 SO4).
Una batería está constituida por un recipiente en el que se alojarán los diferentes componentes, este recipiente tiene una tapa en la parte superior, con unos orificios por los que se introduce el electrólito, además, incorpora dos terminales uno positivo y otro negativo, por los que la conectaremos al automóvil. También en la parte superior lleva una etiqueta donde se detallan las características de la batería. Su interior está dividido en celdas donde se alojan las placas.
1.1.1.- Monobloque y tapa.
A continuación describiremos los componentes externos de un acumulador.
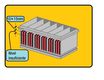
- Monobloque.
El monobloque es un recipiente de polipropileno, material plástico resistente a la corrosión y de gran resistencia mecánica a los impactos y vibraciones. Interiormente está dividido mediante unos tabiques, en celdas o vasos. Para las baterías de 12 voltios el monobloque está divido en 6 vasos. En la parte inferior tenemos unos nervios que sirven de apoyo a las placas y dan rigidez a la batería, además, impiden que el material depositado en el fondo, desprendido de las placas, provoque un cortocircuito.

- Tapa.
Cierra el monobloque por su parte superior y está fabricado del mismo material que él. Tiene un orificio por cada uno de los vasos por el que se le introduce el electrolito para la primera carga e introducir agua destilada en el posterior mantenimiento, este orificio lleva una marca como testigo para indicar el nivel máximo al que puede llegar el electrolito en el proceso de llenado.
Cada orificio lleva un tapón con un pequeño orificio por donde salen los gases producidos en la reacción química, durante la carga y descarga.
La tapa cuenta dos orificios uno en cada extremo, por el que salen al exterior los bornes, uno positivo y otro negativo.
En la tapa viene incorporada una pegatina donde se indican las características de la batería.
1.1.2.- Placas y separadores.
Siguiendo con los componentes de un acumulador veremos los elementos internos.
- Placas.
Las placas positiva y negativa son similares, tienen forma de rejilla y sirven de soporte para la materia activa.
La rejilla de placa positiva está fabricada de una aleación de plomo y antimonio. El antimonio le aporta dureza y le da resistencia a los ataques del acido sulfúrico. La rejilla se empasta con peróxido de plomo (PbO2) como materia activa.
El material utilizado en la fabricación de la rejilla negativa es el plomo aleado con antimonio, en las baterías de bajo mantenimiento se sustituye el antimonio por calcio que origina una menor autodescarga. Como materia activa se utiliza el plomo esponjoso (Pb).
- Separadores.
Los separadores se colocan entre placa y placa. Tienen la misión de impedir el contacto entre ellas y evitar cortocircuitos que se pueden producir por las vibraciones y alabeos de las placas.
Los separadores se fabrican de materiales aislantes y porosos como la fibra de vidrio o polietileno entre otros, que permiten la circulación del electrólito y facilitan un buen contacto de este con la materia activa de las placas.
1.1.3.- Elementos.
¿Sabías que una batería estaba formada por vasos o elementos?
Un elemento está formado por un determinado número de placas positivas y negativas intercaladas, siempre se coloca una placa negativa más. El tamaño y número de placas a colocar en cada elemento depende de la capacidad de la batería, ya que a mayor número de placas mayor cantidad de materia activa para reaccionar.
Las placas de un mismo signo van unidas entre sí mediante un puente e intercaladas con las del signo contrario y entre medio de las dos se coloca el aislante o separador.
El elemento así formado proporciona una tensión de 2,2 voltios, tensión debida al potencial electroquímico.
Para conseguir la tensión de 12 voltios en una batería de acumuladores es necesario la unión de seis elementos.
1.1.4.- Electrólito y la electrólisis.
Alguna vez oíste hablar del agua de las baterías, y sabias que no se trata de agua, sino de una solución ácida.
- Electrólito.
El electrólito líquido empleado en un acumulador de plomo es una solución ácida formada por ácido sulfúrico en un 36%, mezclado con agua químicamente pura en un 64%, la densidad (δ) del ácido sulfúrico (H2 SO4) es de 1,83 g/cm3, que diluido en agua (H2O) de densidad 1 g/cm3 nos da una densidad entre 1,27 y 1,29 g/cm3, densidad que tiene una batería a plena carga.
- Electrólisis.
Electrólisis o separación por electricidad es un método de separación de los elementos que forman un compuesto aplicándole electricidad, este compuesto se disocia en iones, cationes si son iones positivos y aniones si son iones negativos.
El proceso electrolítico es el siguiente: En un recipiente que contiene una disolución acuosa de un ácido, base o sal, introducimos dos electrodos conectados a una fuente de corriente continua, hacia el electrodo positivo o ánodo se dirigen los aniones (iones con carga eléctrica negativa) y hacia el polo negativo o cátodo se dirigen los cationes (iones con carga eléctrica positiva) procedentes de la disociación o (procedentes de la descomposición de la disolución).
Entre los electrodos y los iones se produce una transferencia de electrones, como consecuencia se producen nuevas sustancias.
Antes de pasar al punto siguiente es interesante que visites la siguiente dirección, en la que encontraras una animación que te explica el funcionamiento de una batería.
1.2.- Proceso de descarga de una batería.
¿Sabes que durante el proceso de trabajo una batería se descarga? El proceso lo estudiaremos a continuación.
Para la explicación del proceso de descarga de la batería consideraremos un sólo elemento formado por dos placas, una positiva y otra negativa.
Partimos que la batería está totalmente cargada, en este estado las placas se encuentran con la siguiente composición química; la placa positiva formada por peróxido de plomo (PbO2) y la negativa por plomo esponjoso (Pb) y el electrólito formado por ácido sulfúrico (H2SO4) más agua (H2O). En estas condiciones el acumulador presenta una diferencia de potencial entre los bornes, poniéndose de manifiesto al conectar un polímetro entre los bornes de la batería.
En el momento de cerrar el circuito mediante un consumidor, comienzan a fluir electrones de una forma espontánea desde el polo negativo hacia el polo positivo a través del consumidor, (sentido real de la corriente) y por el interior de la batería del polo positivo al negativo. Esta circulación de corriente provoca la disociación de la molécula de ácido en: un ion sulfato (SO-24) y dos iones hidrógeno (2H+). El sulfato se va hacia las dos placas, formándose en la superficie sulfato de plomo (PbSO4) y liberando oxígeno (O2) de la placa positiva al electrólito que uniéndose con el hidrógeno (H2) forman una molécula de agua (H2O). Este proceso se va repitiendo mientras dura la descarga hasta que se produce casi la totalidad de la disociación del ácido. La descomposición del ácido implica que el electrólito pasa a ser agua casi en su totalidad, disminuyendo la densidad del electrólito y aumentando su resistencia eléctrica.
1.3.- Proceso de carga de una batería.
Igual que a la batería de tu MP3 a la batería de un vehículo es necesario recargarla, el proceso de carga lo estudiaremos en el siguiente apartado.
En el proceso de carga las reacciones químicas se producen de forma inversa a la descarga, para ello conectamos un cargador en paralelo con la batería, es decir, el polo positivo y el negativo del cargador con el polo positivo y negativo de la batería, respectivamente, haciendo pasar corriente por el electrólito.
En la carga el paso de la corriente por el agua del electrólito la descompone formándose los iones peróxido (O-22) e hidrógeno (H+). El oxígeno reacciona con el plomo (Pb) de la placa positiva formándose de nuevo peróxido de plomo y liberando el ión sulfato (SO-24) que reaccionara con el hidrógeno (H+) que quedó libre en la descomposición del agua, formándose la molécula de ácido sulfúrico (H2SO4). En la placa negativa el paso de los electrones descompone el sulfato de plomo (PbSO4), liberando el sulfato (SO-24) y pasando a formar parte del electrólito que uniéndose al hidrógeno (H+) pasa a formar ácido sulfúrico (H2SO4).
Progresivamente en el proceso de carga, la densidad del electrólito va aumentando. Está densidad nos servirá de indicador del estado de carga de la batería.
1.4.- Características eléctricas de una batería.
¿En qué te fijas cuando comparas dos baterías?
Las características eléctricas de un acumulador vienen determinadas por la tensión, la capacidad, capacidad nominal, corriente de cortocircuito, reserva de capacidad, el rendimiento eléctrico y la resistencia interna.
Algunas de estas características vienen indicadas en la batería en una pegatina colocada en la tapa del monobloque.
1.4.1.- Tensión.
¿Cómo pides las pilas de tus aparatos eléctricos: cámara de fotos, mp3, etc.? Lo primero que indicas es la tensión y a continuación el tamaño.
En la batería podemos distinguir tres tipos diferentes de tensión: fuerza electromotriz, tensión eficaz en bornes y tensión nominal.
- Fuerza electromotriz (fem). Es la tensión en bornes de un acumulador, medida con un voltímetro, sin que esté suministrando corriente a un circuito exterior. Esta tensión es la debida a su potencial electroquímico en los acumuladores utilizados en automoción de plomo ácido es de 2,2 voltios por elemento, llegando a un total de 13,2 voltios, ya que están formado por 6 elementos.
- Tensión eficaz en bornes. Es la tensión en bornes una vez que el acumulador se conecta a un circuito exterior, siendo menor que la (fem) debido a la resistencia interna del elemento (resistencia de la placa, resistencia de contacto entre electrólito-paca y resistencia del electrólito). Estas resistencias hacen que al paso de la corriente se produzca una caída de tensión que se restara a la (fem), motivo por el cual la tensión eficaz será menor que la fuerza electromotriz. Su valor lo determinamos con la siguiente expresión:
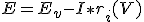
Siendo:
E = tensión eficaz en voltios (V).
Ev= tensión en vacío (V).
ri = resistencia interna (Ω).
I = corriente de descarga (A).
- Tensión nominal. Es la tensión indicada por el fabricante en la placa de características del acumulador y la tensión a la cual funcionan los elementos eléctricos del vehículo. Esta tensión viene determinada por el número de elementos del acumulador, en los acumuladores para arranque es de 6 vasos, siendo la tensión nominal de 12 voltios.
1.4.2.- Capacidad.
Si vas a una tienda de repuesto del automóvil verás baterías de diferente tamaño, ¿sabes porque son diferentes?
La capacidad está ligada a las características constructivas del acumulador, a la cantidad de materia activa, o lo que es lo mismo, tamaño y número de placas.
La capacidad es la cantidad de electricidad que es capaz de suministrar desde plena carga hasta que está completamente descargada. Este valor se expresa en amperios-hora (Ah).
Está capacidad dependa del los siguientes factores:
- Material utilizado en la fabricación de la sustancia activa y cantidad de sustancia activa. A más materia activa, más sustancia para reacciona y por tanto mayor capacidad.
- Espesor de las placas; podemos tener dos baterías con la misma capacidad con placas de diferente espesor, siempre que tengan la misma cantidad de materia activa, menos placas y más gruesas o más placas pero más finas.
La diferencia entre un tipo de placas y otro radica en la necesidad de tener más intensidad en el momento del arranque. Las baterías de arranque tienen que suministra una gran cantidad de corriente para poner en marcha el motor térmico. En este tipo de baterías colocamos placas de poco espesor que permiten que el electrólito penetre de forma más rápida y de una manera más profunda.
- La porosidad y diseño de las placas es fundamental para que el electrólito reaccione con la mayor cantidad de materia activa y no sólo en la superficie.
- Del régimen de descarga: cuanto más lento sea el régimen de descarga mayor rendimiento. La capacidad nominal indica la corriente que un acumulador puede suministra durante 20 h. antes que su valor baje de 10,5 voltios.
- De la temperatura: la capacidad disminuye con las bajas temperaturas, disminuyendo la capacidad hasta el 55% con temperaturas de -18ºC.
El cálculo de la capacidad lo efectuamos con la siguiente expresión:

Capacidad = Intensidad por tiempo, en donde (C) es la capacidad expresada en amperios hora (Ah), (I) es la intensidad en amperios y (t) es el tiempo en horas.
1.4.3.- Capacidad nominal.
Siempre que compramos equipos eléctricos observamos una pegatina, en ella el fabricante nos indica todas las características eléctricas necesarias.
Es la capacidad de la batería, indicada por el fabricante en amperios-hora.
Una batería nueva, cargada al máximo y a una temperatura ambiente de 25ºC, soportando una descarga en 20h su tensión no debe bajar de 10,5V.
Ejemplo:
Tomamos una batería de 80Ah.
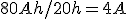
- Una batería de 80 Ah debe entregar durante un mínimo de 20 h una corriente de descarga de 4 A, sin que su tensión descienda por debajo de 10,5 voltios.
Otra característica relacionada con la capacidad del acumulador es: la reserva de capacidad, que la definimos como la habilidad de una batería para mantener la carga eléctrica de la batería en un valor mínimo. En el caso que falle el sistema de carga. Esta corriente mínima debe ser capaz de encender las luces delanteras, el arranque, el limpia parabrisas; consumiendo aproximadamente 25 amperios.
Capacidad de reserva es el tiempo en minutos que un acumulador nuevo a plena carga y a una temperatura de 27ºC puede descargarse de manera continua y mantener un voltaje igual o mayor de 1,75 voltios por celda.
1.4.4.- Corriente de cortocircuito y rendimiento eléctrico.
Otra de las características de un acumulador es la corriente de cortocircuito.
- Corriente de cortocircuito.
La corriente de cortocircuito o intensidad máxima de descarga (Icc) indica la intensidad máxima que el acumulador puede proporcionar en un momento dado. Esta intensidad viene indicada en la placa de características del acumulador.
Su valor se obtiene dividiendo la tensión en bornes de la batería por su resistencia interna.
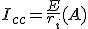
En donde:
Icc= Corriente de cortocircuito.
E= Tensión en bornes.
ri= Resistencia interna.
- Rendimiento eléctrico.
El rendimiento eléctrico (η) viene expresado por la relación entre la energía capaz de suministrar durante la descarga y la energía consumida durante la carga.

En donde:
η = rendimiento expresado en tanto por ciento.
Wd = energía de descarga.
Wc = energía de carga.
1.4.5.- Resistencia interna.
Los acumuladores como todos los elementos eléctricos tienen resistencia, ¡OJO! No la midas con un polímetro no se puede.
La resistencia interna de un acumulador depende de varios factores como la resistencia de las placas, la resistencia de contacto entre placa y electrólito, la resistencia de los puentes de unión entre placas y entre elementos y sobre todo de la resistencia del electrólito.
De los diferentes factores, solamente tenemos en cuenta para el cálculo la resistencia interna, la resistencia del electrólito, cuyo valor depende de la concentración y esta está en función del estado de carga.
- Cálculo de la resistencia interna de un acumulador:
Para el cálculo de la resistencia del electrólito utilizamos la siguiente expresión:


Siendo:
Rit = resistencia interna total.
N= número de elementos.
Ri=resistencia interna.
Re=resistencia del electrólito (inversa de la conductibilidad).
Sp=superficie de una de las caras de la placa en cm2.
d=separación entre placas en cm.
Np=número de placas positivas de cada elemento.
ξ=conductibilidad del electrólito por cm3.
2= se pone en la ecuación por las dos caras activas de las placas positivas.
2.- Manipulación y comprobación de una batería.

-Lorenzo ayer estuve mirando el nivel de electrólito de la batería de un amigo, en uno de los vasos le faltaba un poco de agua.
-María, le echarías agua destilada, ya sabes que el agua del grifo no es la adecuada.
Como ya sabes la batería necesita una revisión periódica al igual que muchos elementos del vehículo, con esta revisión pretendemos alargar al máximo la vida de la batería en un buen estado de funcionamiento y fiabilidad.
La batería a lo largo de su vida útil, necesita un mantenimiento. Para realizar este mantenimiento es necesario tener presente ciertas precauciones a la hora de manipular una batería, ya que, una manipulación inadecuada, puede ocasionar daños tanto al vehículo como al operario que realiza el trabajo.
Es necesario utilizar los equipos de protección personal (EPI); en los trabajos con acumuladores debemos utilizar guantes y gafas, para evitar las salpicaduras del ácido.
2.1.- Sustitución de la batería.
Has de tener en cuenta una serie de cuestiones en el momento de sustituir una batería por agotamiento, para realizar el mantenimiento o una reparación en el vehículo debemos de seguir un proceso:
| 1 | A la hora de sustituir una batería tenemos que asegurarnos que la nueva batería cumpla las características de la vieja, un parámetro muy a tener en cuenta es la capacidad, porque de ello depende la puesta en marcha del motor, nunca debemos montar una batería con menor capacidad porque en muchos casos no arrancará el motor. Una capacidad superior no entraña ningún problema siempre que quepa en su alojamiento. |
|---|---|
| 2 | Muchos vehículos cuentan con componentes que al desconectarle la corriente se desprograman, por lo tanto en algunos casos se monta otra batería en paralelo antes de desconectar la batería a sustituir. |
| 3 | En primer lugar, desconectamos el borne de masa, para evitar posibles cortocircuitos. En el caso de quitar en primer lugar el borne positivo, si tocamos con la llave el tornillo del terminal y a su vez la llave toca en una parte metálica del coche, se producirá un corto circuito, porque cerraríamos el circuito a masa; este es el motivo por el que en primer lugar se quita el negativo. A continuación podemos quitar el terminal positivo. |
| 4 | Antes de montar la nueva batería, debemos limpiar el alojamiento de posibles restos de electrólito, de óxido y restos de sulfatación. También limpiaremos los terminales. |
| 5 | En el momento de colocar la nueva batería nos debemos asegurar de no equivocarnos en la polaridad, ya que, podríamos destruir alguno de los componentes electrónicos muy abundantes en los vehículos actuales. Colocaremos en primer lugar el borne positivo y a continuación el negativo, siguiendo el sentido inverso al desmontaje. |
2.2.- Comprobación de la batería mediante el densímetro (I).
Cuando cargues una batería recuerda que tienes que verificar su estado de carga.
Siempre que hemos sometido una batería a un proceso de carga fuera del vehículo es necesario realizar una comprobación, podemos realizarla con tres métodos diferentes:
- Densímetro o hidrómetro.
- Polímetro.
- Comprobador de descarga rápida.
Como vimos al estudiar el proceso químicos de carga y descarga, la densidad del electrólito variaba con el estado de carga. De esta densidad nos serviremos para determinar el estado de la batería.
Una batería cuando está totalmente cargada su densidad oscila entre 1,27 y 1,29 g/cm3 y consideramos descargada cuando se encuentra entre 1,11 y 1,30 g/cm3, por lo tanto en estados intermedios de densidad tendrá estados intermedios de carga.
Antes de proceder a la comprobación de la batería hay que tener en cuenta algunas cuestiones:
- Nivel del electrólito debe ser el correcto, aproximadamente 1 cm por encima de las placas.
- Dejar reposar la batería antes de realizar la medición, consideramos que está en reposo cuando han pasado 4 horas de haber sido retirada del cargador.
- No medir inmediatamente después de haber rellenado con agua destilada.
- Si la temperatura difiere de 25ºC hacer las correcciones necesarias.
Antes de comenzar con el proceso de comprobación describiremos el hidrómetro o pesa ácidos.
Consta de:
- Tubo transparente de vidrio o plástico resistente al ácido.
- Boquilla para introducirla por el orificio de llenado de los diferentes vasos.
- Pera de goma para provocar la aspiración y poder llenar el tubo con el electrólito.
2.2.1.- Comprobación de la batería mediante el densímetro (II).
En el interior de este tubo tenemos una bolla con una escala graduada, está bolla flotará más o menos, según la densidad. Algunos modelos cuentan con dos escalas, una en g/cm3 y otra en tanto por ciento (%).
Antes de quitar los tapones, limpiaremos la batería para evitar que se introduzca suciedad que pueda alterar la reacción química o producir cortocircuito.
Pasos a seguir para la correcta utilización del densímetro:
- Succionar con la pera hasta que la bolla pueda flotar libremente.
- Colocar el densímetro vertical para que el flotador no roce con las paredes del tubo y false la medida.
- Proceder a la medida, mirando hasta que nivel flota la bolla, esta será la medida de la densidad.
- Devolver el electrólito a su vaso y repetir el proceso en los demás vasos. Si la medida de uno de los vasos difiere de los otros una cantidad igual o superior a 0,030 g/cm3, consideramos que la batería está en mal estado.
- Realizamos la corrección de la densidad según la temperatura de la siguiente manera; por cada 5ºC por encima o por debajo de los 25ºC sumamos o restamos 0,0035 unidades a la lectura de la densidad, si está por encima, sumamos y si está por debajo, restamos esa cantidad.
| Densidad a 25ºC | Carga |
|---|---|
| 1,270-1,290 | 100% |
| 1,230-1,250 | 75% |
| 1,200-1,220 | 50% |
| 1,170-1,190 | 25% |
| 1,140-1,160 | Poca capacidad |
| 1,110-1,130 | Descargada |
2.3.- Comprobación de la batería mediante el polímetro.
No olvides el multímetro, es una herramienta indispensable para un mecánico.
El polímetro es un instrumento de medida que nos permite determinar el estado de carga, con el se puede medir la tensión en bornes, pero no el estado de envejecimiento de la batería.
Para comprobar el estado de carga de una batería después de haber estado conectada a un cargador es necesario esperar un mínimo de 4 horas.
La tensión indicada en el polímetro debe ser igual o superior a 12,7 voltios y si la tensión es inferior indicara que la batería esta en mal estado.
La tabla siguiente nos relaciona la tensión en bornes medida con el polímetro y el estado de carga de la batería, se puede apreciar que una pequeña variación de tensión supone una variación importante en el estado de carga de la batería.
| Tensión de bateria (V) | Estado de carga (%) |
|---|---|
| 12,60 voltios o más | 100% |
| 12,50-12,45 voltios | 80% |
| 12,35-12,25 voltios | 50% |
| 12,15-12,00 voltios | 25% |
| 11,70 voltios o menos | 0% |
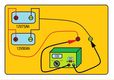
2.4.- Comprobación de la batería mediante el comprobador de descarga rápida.
Sabías qué el comprobador de descarga es quizás la mejor herramienta para comprobar el estado de un acumulador.
Las pruebas del estado de carga mediante un comprobador someten a la batería a una descarga violenta, semejante a la que es sometida en el momento del arranque. El comprobador provoca descargas del orden de 250 A, por este motivo es una prueba a la que no se debe someter a la batería de forma repetida, ya que podemos deteriorarla.
Para la comprobación seguimos el siguiente proceso:
- Conectamos las pinzas de alimentación a los terminales, pinza roja al positivo.
- Consultamos el polímetro digital.
- Comparamos la lectura con la tabla de carga de la batería.
- Sí la tensión es inferior a 12,35 voltios, cargar la batería durante 15 minutos.
- Conectamos la pinza de 250 A, a un terminal de la batería.
- Con la punta-pulsador hacemos presión sobre el otro terminal hasta que el indicador verde se apague, en ese momento habrán trascurrido 10 segundos.
- La lectura del polímetro durante la prueba no debe ser inferior a 9,00 voltios y sí supera esta tensión, la batería está en buen estado y sí no, está defectuosa.
El comprobador cuenta con un testigo de seguridad para evitar sobrecalentamientos, si el testigo de seguridad se ilumina, es necesario detener la prueba hasta que este se apague de nuevo.
2.5.- Carga de la batería.
Como ya vimos anteriormente las baterías las baterías necesitan cargas periódicas para mantenerlas en un perfecto estado de mantenimiento.
La batería fuera de servicio sufre una autodescarga progresiva, por este motivo es necesario recargarla para mantenerla en un buen estado de conservación. También puede descargarse por un mal funcionamiento del circuito de carga, en este caso es necesario su recarga.
Antes de poner en carga una batería debemos tener presentes una serie de recomendaciones:
| Recomendaciones de seguridad | Recomendaciones para realizar una carga correcta | ||
|---|---|---|---|
| 1 | El lugar donde se realiza la carga debe ser fresco y estar bien ventilado. | A ser posible hacer una carga lo más lenta posible. | 1 |
| 2 | No colocar el cargador en lugares donde le puedan llegar los vapores procedentes de la batería, ya que son muy corrosivos. | Si es necesario rellenar con agua destilada hasta el nivel necesario o entre 10 y 15 milímetros por encima de las placas. | 2 |
| 3 | Conectar las pinzas a los bornes de la batería con el cargador desconectado para evitar el deterioro de los bornes por el chisporroteo. | Limpiar los bornes y la parte superior de la batería, antes de quitar los tapones para evitar que caiga suciedad en el interior. Los tapones deben permanecer quitados durante la carga. | 3 |
| 4 | No acerca ninguna llama u objeto incandescente a la batería para evitar explosiones, debido al hidrógeno que se desprende del electrólito durante la carga. | ||
| 5 | Para desconectar las pinzas de los bornes antes es necesario desconectara el cargador. | ||
2.6.- Sistemas de carga.
¿Te has preguntado cómo se carga una batería?
Los aparatos utilizados para realizar la carga fuera del vehículo constan de un sistema rectificador de corriente y un transformador.
Podemos utilizar dos sistemas de carga: uno lento y otro rápido, el sistema rápido es el menos adecuado por someter a la batería a un paso de intensidad elevado y sólo es adecuado cuando la batería está en muy buen estado. Con el sistema lento de carga, los iones cuentan con más tiempo para reaccionar, por consiguiente, las baterías sufren menos, puesto que, no aumentan tanto la temperatura.
La intensidad máxima de carga debe ser del 10% de la capacidad nominal de la batería. Por ejemplo si tenemos una batería de 75Ah de capacidad, colocaremos el selector de intensidad de carga a un máximo de 7,5A.
En el mercado contamos con diferentes tipos de cargadores, cuya mayor diferencia es la potencia y la automaticidad de la cargas. Algunos cargadores cuentan con sistemas para poder cargar la batería colocada en el automóvil sin riesgo para los sistemas electrónicos, debido a los picos de tensión. También podemos encontrarlos con ayuda al sistema de arranque y con comprobador de alternador.
Para cargar dos baterías a la vez podemos conectarlas en: serie o paralelo. Para determinar cuál de las dos opciones es la correcta, en cada caso, debemos tener en cuenta la tensión nominal de cada una, la capacidad y el estado en que se encuentran.
- Se cargaran:
- En serie, cuando las dos baterías tengan distinta tensión.
Seleccionaremos la intensidad de carga, teniendo en cuenta la capacidad de la batería menor.
- Colocaremos el selector de tensión en 24voltios, que es la suma de la tensión nominal de las dos baterías.
- En paralelo, cuando su nivel de descarga se similar.
- Seleccionamos la intensidad de carga teniendo en cuenta la suma de las capacidades y aplicando el 10%.
- Colocamos el selector de tensión en 12 voltios que es la tensión nominal de un de las baterías.
- En serie, cuando las dos baterías tengan distinta tensión.
De una manera general. Los pasos a seguir en el proceso de puesta en carga, son los siguientes:
- En baterías con mantenimiento, quitar los tapones.
- Conectar las pinza respetando la polaridad.
- Colocar el selector de tensión de carga en 12V ó 24V; en 24V si conectamos 2 baterías en serie.
- Colocar el selector en posición de (TEST) y comprobar la polaridad y el estado de carga (tensión).
- En un proceso de carga normal, colocar el selector en la primera posición de carga donde la intensidad de carga es menor.
- Para realizar una carga rápida, colocar el selector en la 2ªposición, donde la intensidad será mayor y colocar el selector de tiempo en 60 minutos.
- Una vez seguido todos los pasos podemos conectar el cargador.
2.7.- Mantenimiento de los acumuladores.
¿Sabes cómo puedes prolongar la vida de una batería? Siguiendo unos consejos muy sencillos puedes conseguirlo.
Las baterías durante los procesos de carga y descarga van reduciendo su capacidad de reacción debido a que parte del sulfato que se produce en las placas se vuelve irreductible, perdiendo su capacidad de reacción, además parte de la materia activa de las placas que se desprende de ellas se deposita en el fondo, quedando inutilizada.
Es posible prolongar la vida de nuestras baterías siguiendo un proceso de mantenimiento muy sencillo.
En la tabla siguiente enumeramos seis puntos a tener en cuenta en el mantenimiento de los acumuladores, con estas recomendaciones se puede prolongar la vida de las baterías.
| 1º | Mantenerla siempre cargada. |
|---|---|
| 2º | No sobrecargarla ni descargarla en exceso. |
| 3º | No someterlas a descargas intensas un tiempo prolongado. |
| 4º | No someterlas a temperaturas extremas. |
| 5º | Reponer el agua destilada que pierda. |
| 6º | Nunca reponer con ácido sulfúrico. |
2.8.- Causas que limitan la vida de una batería.
Las baterías desde el mismo momento de añadirle el ácido comienza su envejecimiento, este envejecimiento se puede acelerar por los motivos que se detallan a continuación:
- Efectos producidos por una carga excesiva.
Sí a una batería que se encuentra con una carga próxima al 100% le seguimos suministrando corriente de carga, provocará que el agua descompuesta en gas hidrógeno y oxígeno se escapen del electrólito en forma de burbujas (gasificación), disminuyendo el nivel de este y en consecuencia, aumentando la concentración, con el consiguiente peligro de destrucción por la disolución del plomo de la materia activa y del armazón.
Este exceso de corriente de carga hará que siga descomponiéndose el agua del electrólito, el oxígeno liberado al no encontrar materia activa para reaccionar lo hará con el plomo de las placa positiva, oxidándola y debilitándola, con el consiguiente peligro de rotura. El hidrógeno liberado sale al exterior en forma de burbujas con peligro de explosión.
Esta sobrecarga en vehículos en servicio, generalmente, se debe a un defecto del regulador, y en las baterías sometidas a carga fuera del vehículo a un exceso de intensidad de carga y aún tiempo excesivo.
- Efectos producidos por una descarga excesiva.
Estas descargas prolongadas provocan en la batería una disminución de la capacidad, siendo incapaz de poner en marcha el vehículo, en una descarga profunda el sulfato de plomo se puede volver irreductible, no siendo capaz de revertir el proceso en su totalidad durante el proceso de carga. Este fenómeno se le llama sulfatación.
- Falta de agua.
Como hemos visto anteriormente, las reacciones químicas descomponen el agua en sus 2 componentes oxígeno e hidrógeno y parte de estos se liberan al exterior, con la consiguiente pérdida de agua, quedando las placas por debajo del nivel del electrólito. Esta porción de placa se sulfata con un sulfato duro e irreductible.
3.- Evolución de las baterías de arranque.
María y Lorenzo charlan sobre las baterías de nueva aparición en el mercado, de los diferentes tipos de baterías y de su duración.

Como habrás podido comprobar las baterías siguen una evolución paralela a la aparición de los nuevos materiales de fabricación y a las nuevas tecnologías.
Con los nuevos materiales se consigue un mejor rendimiento de la batería en cesión de la energía a baja temperatura también un mayor ciclo de cargas/descargas y un menor mantenimiento por perdida de agua.
Antes de pasar al punto siguiente es interesante que visites la siguiente dirección, en la que encontraras una presentación que te hablará de los diferentes tipos de pilas y baterías.
3.1.- Baterías de bajo mantenimiento y libres de mantenimiento.
En el mercado podemos encontrar diferentes tipos de baterías en este apartado estudiaremos dos clases.
- Baterías de bajo mantenimiento.
Con este tipo de baterías se consigue una menor autodescarga y una menor pérdida de agua.
Las baterías de plomo ácido usan para la fabricación de las rejillas, una aleación de plomo puro y antimonio, este último utilizado para darle mayor resistencia mecánica pero es el metal que produce la autodescarga y la pérdida de agua. En las baterías de bajo mantenimiento reducimos la utilización de antimonio, sustituyéndolo por calcio que provoca una menor autodescarga y pérdida de agua.
- Baterías sin mantenimiento.
Se caracterizan porque no necesitan que se les agregue agua durante su vida de funcionamiento.
Las aleaciones de plomo y antimonio generan calor con la corriente de carga, aumentando la resistencia interna de la batería, como consecuencia, aparece la perdida de agua por evaporación.
La aleación de plomo y calcio tiene mejor conductibilidad, permitiendo a la batería tener un 20% más de capacidad que las que utilizan antimonio.
El calor, la pérdida de agua y la gasificación se reducen en la batería que no requiere mantenimiento.
En algunas baterías libres de mantenimiento, las rejillas se fabrican con aleaciones de Calcio-Plata que mejoran la resistencia a la corrosión.
3.2.- Baterías AGM.
A continuación estudiaremos otro tipo de batería.
En las baterías AGM el electrólito no es líquido. Son las que llamamos baterías secas, en este caso, el electrólito está fijo a los separadores. Estos separadores se fabrican de fibra de vidrio con gran capacidad de absorción, cuyas siglas en ingles son (AGM) Absorbed Glass Mat.
En su construcción, al agregarle el electrólito líquido, es absorbido por el separador y fijado a él. No es necesario agregarle agua; en estas baterías se produce una recombinación de los gases, formándose de nuevo agua.
Tiene unos tapones que actúan como válvulas, permitiendo salir los gases cuando hay una presión excesiva. Estas baterías las podemos colocar acostadas sin que por ello pierdan el electrolito.
Estas baterías se han de cargar teniendo cuidado con la intensidad de carga, que si es excesiva, provoca una excesiva gasificación, llegando a deteriorar la batería. Es recomendable no exceder en la intensidad de carga el 10% de su capacidad.
Las baterías AGM tienen alta resistencia a ciclos de carga y descarga; cuentan con buenas propiedades para el arranque en frío en su contra no son adecuadas para trabajar en ambientes con temperaturas elevadas.
3.3.- Baterías de GEL.
¿Existe una batería de gel? Si y si quieres saber más de este tipo de batería sigue este apartado con atención.
A estas baterías, en el electrólito, se le añade un compuesto de silicona, provocando que el líquido se vuelva una masa sólida e impidiendo que el electrólito se derrame en el caso de una rotura del monobloque.
Están selladas herméticamente, los gases producido con las reacciones químicas se recombinan formando de nuevo agua, por tal motivo no es necesario añadirle agua desmineralizada.
Las placas positiva y negativa, están fabricadas de aleación plomo-calcio. La placa positiva es más gruesa.
Tiene muy baja autodescarga, pueden conservar un 80% de su capacidad nominal hasta los 6 meses y un 60% hasta los 2 años, y alta resistencia a los ciclos alternativos de carga y descarga.
Esta batería cuenta con algunos inconvenientes como mala prestación en el arranque en frio y el precio es más elevado.
3.4.- Baterías de níquel e hidruros metálicos.
Este tipo de baterías son las más utilizadas en los vehículos híbridos.
Los acumuladores para los vehículos híbridos necesitan tener un gran número de celdas, ya que tienen que proporcionar alta tensión para poder mover el vehículo, mediante un motor eléctrico alimentado por la batería.
El ánodo está formado por oxidróxido de níquel y el cátodo es una aleación de hidruro metálico.
Cada célula de Ni-MH puede proporcionar un voltaje de 1,2 voltios y una capacidad de 0,8 a 2,9 Ah.
Estas baterías tienen una densidad de energía (energía por unidad de peso), de 80 Wh/Kg.
- Ventajas:
- Larga vida en ciclos de carga y descarga de 2000 ciclos.
- Puede almacenarse en bajo estado de carga.
- Buenas prestaciones a alta potencia, tanto en carga, como en descarga, incluso en bajo estado de carga.
- Tiene poco efecto memoria.
- Inconvenientes:
- Moderada prestación a bajas temperaturas.
- Coste elevado.
- Precisa control de presión y temperatura al final de la carga.
3.5.- Baterías de iones de litio.

¿Sabías que uno de los inconvenientes de estas baterías es el peligro de explosión?
En las baterías de iones de litio el electrodo positivo (ánodo) está formado por grafito y el negativo (cátodo) por aleaciones de litio con cobalto o magnesio.
- Durante la descarga los iones de litio pasan espontáneamente a través del electrólito del cátodo al ánodo, pero no los electrones que circularán por el exterior a través del consumidor del polo negativo al positivo, produciendo trabajo.
- Durante el tiempo que dura la descarga, los iones se dirigen hacia el ánodo. Cuando todos se encuentran en el ánodo la batería se encuentra totalmente descargada.
- Durante la carga aplicamos una tensión en sentido inverso, haciendo que lo iones se desplacen desde el ánodo hasta el cátodo, quedando la batería cargada de nuevo.
- Ventajas:
- Alta densidad energética.
- Baja autodescarga.
- Bajo efecto memoria.
- Larga vida en ciclos de carga y descarga entre 1000 y 1500 ciclos.
- Inconvenientes:
- No admite cargas y descargas excesivas, necesitando un sistema de protección.
- No admiten bien los cambios de temperatura.
- Coste elevado.
3.6.- Pila de combustible.
¿Has oído hablar de la pila de combustible? ¿Te parece interesante?
La pila de combustible NO es un elemento acumulador, sino un convertidor electroquímico de energía, que produce directamente la corriente. Realiza el proceso inverso a la electrólisis, combina oxígeno e hidrógeno para producir electricidad y además, produce una gran cantidad de calor y agua, considerando el agua el único residuo de la reacción.
Este dispositivo no necesita ser recargado, produce corriente eléctrica siempre que le suministremos combustible y oxidante en los electrodos. Como combustible utilizamos hidrógeno, gas natural e hidrocarburos y como oxidante utilizaremos el oxígeno o aire.
El hidrógeno lo introducimos por el electrodo positivo o ánodo, y el oxígeno por el negativo o cátodo.
La celda de combustible está formada por dos electrodos separados por un electrólito através del cual pasan los iones (H+) pero no los electrones (e-), de forma que se crea una diferencia de potencial y por lo cual una fuerza electromotriz entre los electrodos. Esta energía eléctrica se genera por oxidación electroquímica del combustible y la reducción electroquímica del oxidante.
Las celdas tienen una tensión de 1,23 voltios, por tal motivo para alcanzar tensiones más elevadas es necesario conectarlas entre ellas en una conexión en serie.
4.- Acoplamiento de baterías.

En el taller Lorenzo y María tienen la necesidad de comprobar el motor de arranque de un camión y se encuentran con el problema de qué el motor es de 24V y las baterías que tienen son de 12V.
─No te preocupes Lorenzo que acoplo dos baterías en serie y solucionamos el problema.
─Estas en todo, chica. ¿Qué haría yo sin ti?
En el mercado podemos en contra baterías con unas características de tensión y capacidad determinada, por tanto, cuando necesitamos para un montaje unas características concretas tenemos que recurrir al acoplamiento de las baterías.
- Estos acoplamientos pueden ser de 3 tipos:
- Acoplamiento en serie.
- Acoplamiento en paralelo.
- Acoplamiento mixto.
4.1.- Acoplamiento en serie y características de la asociación.
Alguna vez podemos necesitar una tensión distinta a la que nos ofrecen las baterías existentes en el mercado, a continuación veremos cómo podemos obtenerla.
En un acoplamiento en serie debemos conectar el borne negativo de una batería con el positivo de la otra y así sucesivamente, dejando siempre un borne negativo y otro positivo libre, donde conectaremos el dispositivo que queremos alimentar.
Es condición necesaria para poder realizar esta asociación que las baterías tengan la misma capacidad, el motivo es el siguiente: a la hora de conectar un consumidor se descargará antes la batería con menor capacidad y si el proceso de descarga se prolonga hasta agotar la batería de mayor capacidad, la de menor sufriría una descarga excesiva, con los consiguientes problemas ya mencionados en anteriores apartados. En el caso contrario, al cargar las baterías, la de menor capacidad podría sufrir una sobrecarga. Por este motivo durante la carga seleccionaremos la intensidad de carga teniendo en cuenta la capacidad de la menor.
Características eléctricas del la asociación.
- La capacidad.
Al tratarse de un acoplamiento en serie la intensidad que recorre todas las baterías conectadas es la misma, por lo tanto, la capacidad (C), (intensidad por tiempo) se mantiene constante e igual a la de una de las baterías.

- Tensión.
Una asociación en serie de acumuladores, la tensión resultante (Et) es la suma de las tensiones de las diferentes baterías.
Esto es, como si formamos una batería con un número de elementos igual a la suma de todos los que forman los distintos acumuladores.

- Resistencia.
Es la suma de las resistencias de todos los acumuladores.

4.2.- Acoplamiento en paralelo y características de la asociación.
Como dijimos anteriormente es probable que en el mercado no encontremos baterías con unas características muy determinadas, por este motivo es necesario realizar diferentes tipos de acoplamientos.
El acoplamiento de baterías en paralelo lo realizamos uniendo los bornes negativos y positivos, respectivamente, de todas las baterías. Para la toma de corriente conectamos por un lado en el borne positivo y por el otro en el negativo.
Para poder realizar esta asociación es preciso que todos los acumuladores conectados tengan la misma tensión, de lo contrario, el de mayor tensión actuaría de cargador sobre los demás.
Características eléctricas del la asociación.
- Capacidad.
Al acoplarlas en paralelo es equivalente a colocar en un elemento un número de placas positivas y negativas, igual a la suma de todas las placas positivas y negativas respectivamente.
La capacidad total es la suma de las capacidades.
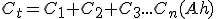
- Tensión.
En un acoplamiento en paralelo todos los bornes positivos con respecto a los negativos se mantienen al mismo potencial.
La tensión obtenida por medio de este acoplamiento, es constante e igual a la de una batería.
Et=E1=E2=E3... En (V)
- Resistencia.


Si todos los acumuladores tienen la misma resistencia:
Donde:
Rt = resistencia total.
N = número de baterías.
Ri = resistencia interna de una batería.


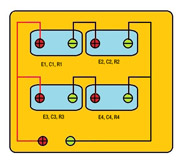
4.3.- Acoplamiento mixto.
Esta es otra de las formas de acoplar las baterías.
Para realizar estos acoplamientos conexionamos las baterías en serie y en paralelo conjuntamente.
Indistintamente, podemos unirlas formando asociaciones en serie y estas con otras en paralelo o viceversa. Las distintas conexiones las realizaremos en función de las características que queremos conseguir.
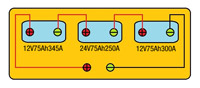
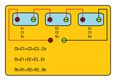
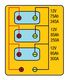
4.3.1.- Acoplamiento serie-paralelo.
Se dispone de 3 baterías con las siguientes características:
- 6V 75Ah 345A.
- 6V75Ah 250A.
- 12V90Ah 300A.
- Calcula:
- Capacidad.
- Tensión total si se conectan en serie-paralelo.
- Las 2 primeras en serie con la 3ª en paralelo.
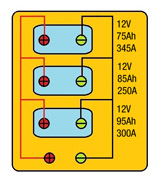
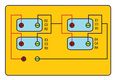
4.3.2.- Acoplamiento paralelo-serie.
Se dispone de 3 baterías con las siguientes características:
- 24V 175Ah 345A.
- 12V85Ah 250A.
- 12V90Ah 300A.
- Calcula:
- Capacidad.
- Tensión total si se conectan en paralelo-serie.
- La primera en serie con las 2 restantes en paralelo.
5.- Normas de seguridad.

Lorenzo y María han ido juntos a comprarse el material de seguridad necesario para las prácticas de la batería.
Lorenzo se ha asegurado que cumplen la homologación para este tipo de trabajo y María se siente orgullosa del trabajo realizado por su compañero.
Ya conoces la importancia que tiene las normas de seguridad para la vida de los trabajadores, por este motivo es necesario respetarlas.
Debido a los materiales que componen los acumuladores y a las reacciones químicas que se producen en su interior, es necesario tomar unas medidas de precaución en su de su manipulación.
- Riesgos en operaciones con baterías:
- Riesgo de contacto y proyección de ácido sulfúrico en el proceso de llenado.
- Riesgo de explosión, ocasionado por el desprendimiento de hidrógeno y oxígeno durante el proceso de carga.
- Riesgos de cortocircuito, por contacto con los bornes con un elemento metálico durante su manipulación.
- Riesgos por inhalación de aerosoles de ácido sulfúrico.
- El mayor riesgo con el ácido se da en el caso de salpicadura a los ojos. En este supuesto se ha de actuar rociando con abundante agua corriente. Como medida de protección en el caso de salpicadura en los ojos se ha de contar con una fuente lavaojos a una distancia máxima de 10 m de los puestos de trabajo.
Los equipos de protección individual (EPI), necesarios para la manipulación de baterías, estará formado por:
- Guantes resistentes a los ácidos.
- Gafas de seguridad.
- Botas de seguridad.
Para la carga de baterías es necesario contar con un local adecuado para este fin. La sala de carga tendrá una ventilación suficiente para evitar la acumulación de gases e impedir que la temperatura ascienda demasiado, favoreciendo la refrigeración de las baterías y cargadores. El local contará con la señalización adecuada.
6.- Reciclaje.

En el taller se ha organizado un seminario sobre prevención de riesgos laborales, María y Lorenzo van de visita a un centro de reciclaje y descontaminación.
En este lugar les dan una charla sobre la necesidad de reciclar y descontaminar los vehículos una vez que llegan al final de su vida útil.
Tan importante como la seguridad del trabajador es la seguridad del medio ambiente. Todos debemos colaborar en preservar la tierra y para ello tenemos que concienciarnos de la necesidad de reciclar los residuos que generamos.
Las medidas medio ambientales con su norma, descrita en el Real Decreto 106/2008, de 1 de Febrero, sobre pilas y acumuladores y la gestión ambiental de sus residuos, pretenden conseguir una buena gestión de los residuos contaminantes y facilitar su recogida, tratamiento y reciclaje.
Se prohíbe la incineración y eliminación en los vertederos de los acumuladores.
La recogida y gestión de los residuos queda recogida en el anterior Real Decreto. Las baterías de automoción, su recogida, la realizará el fabricante o servicios de gestión autorizados sin coste para los usuarios.
El reciclaje de las baterías se realizará en instalaciones autorizadas.
Si estás interesado en conocer más sobre la legislación, del tratamiento de los residuos procedentes de los acumuladores, en esta página podrás informarte.
Anexo.- Licencias de recursos.
| Recurso (1) | Datos del recurso (1) | Recurso (2) | Datos del recurso (2) |
|---|---|---|---|
 |
Autoría: Jesús Pereira Iglesias. Licencia: CC BY-NC 2.0. Procedencia: http://www.flickr.com/photos/chuchipi/6121091582/in/photostream/lightbox/ |
 |
Autoría: Jesús Pereira Iglesias. Licencia: CC BY-NC 2.0. Procedencia: http://www.flickr.com/photos/chuchipi/6121093082/in/photostream/lightbox/ |
 |
Autoría: Jesús Pereira Iglesias. Licencia: CC BY-NC 2.0. Procedencia: http://www.flickr.com/photos/chuchipi/6121091652/in/photostream/lightbox/ |
 |
Autoría: Jesús Pereira Iglesias. Licencia: CC BY-NC 2.0. Procedencia: http://www.flickr.com/photos/chuchipi/6121091876/in/photostream/lightbox/ |
 |
Autoría: Jesús Pereira Iglesias. Licencia: CC BY-NC 2.0. Procedencia: http://www.flickr.com/photos/chuchipi/6121091958/in/photostream/lightbox/ |
 |
Autoría: Jesús Pereira Iglesias. Licencia: CC BY-NC 2.0. Procedencia: http://www.flickr.com/photos/chuchipi/6121092072/in/photostream/lightbox/ |
 |
Autoría: Jesús Pereira Iglesias. Licencia: CC BY-NC 2.0. Procedencia: http://www.flickr.com/photos/chuchipi/6121092160/in/photostream/lightbox/ |
 |
Autoría: Jesús Pereira Iglesias. Licencia: CC BY-NC 2.0. Procedencia: http://www.flickr.com/photos/chuchipi/6121092274/in/photostream/lightbox/ |
 |
Autoría: Jesús Pereira Iglesias. Licencia: CC BY-NC 2.0. Procedencia: http://www.flickr.com/photos/chuchipi/6121092410/in/photostream/lightbox/ |
 |
Autoría: Jesús Pereira Iglesias. Licencia: CC BY-NC 2.0. Procedencia: http://www.flickr.com/photos/chuchipi/6121092512/in/photostream/lightbox/ |
 |
Autoría: Jesús Pereira Iglesias. Licencia: CC BY-NC 2.0. Procedencia: http://www.flickr.com/photos/chuchipi/6121092622/in/photostream/lightbox/ |
 |
Autoría: Jesús Pereira Iglesias. Licencia: CC BY-NC 2.0. Procedencia: http://www.flickr.com/photos/chuchipi/6121093178/in/photostream/lightbox/ |
 |
Autoría: Jesús Pereira Iglesias. Licencia: CC BY-NC 2.0. Procedencia: http://www.flickr.com/photos/chuchipi/6120550841/in/photostream/lightbox/ |
 |
Autoría: Jesús Pereira Iglesias. Licencia: CC BY-NC 2.0. Procedencia: http://www.flickr.com/photos/chuchipi/6121093464/in/photostream/lightbox/ |
 |
Autoría: Jesús Pereira Iglesias. Licencia: CC BY-NC 2.0. Procedencia: http://www.flickr.com/photos/chuchipi/6121093006/in/photostream/lightbox/ |
 |
Autoría: Jesús Pereira Iglesias. Licencia: CC BY-NC 2.0. Procedencia: http://www.flickr.com/photos/chuchipi/6121092726/in/photostream/lightbox/ |
 |
Autoría: Jesús Pereira Iglesias. Licencia: CC BY-NC 2.0. Procedencia: http://www.flickr.com/photos/chuchipi/6121091154/in/photostream/lightbox/ |
 |
Autoría: Jesús Pereira Iglesias. Licencia: CC BY-NC 2.0. Procedencia: http://www.flickr.com/photos/chuchipi/6121092794/in/photostream/lightbox/ |
 |
Autoría: Jesús Pereira Iglesias. Licencia: CC BY-NC 2.0. Procedencia: http://www.flickr.com/photos/chuchipi/6121091250/in/photostream/lightbox/ |
 |
Autoría: Jesús Pereira Iglesias. Licencia: CC BY-NC 2.0. Procedencia: http://www.flickr.com/photos/chuchipi/6121092880/in/photostream/lightbox/ |
 |
Autoría: Jesús Pereira Iglesias. Licencia: CC BY-NC 2.0. Procedencia: http://www.flickr.com/photos/chuchipi/6120548841/in/photostream/lightbox/ |
 |
Autoría: Jesús Pereira Iglesias. Licencia: CC BY-NC 2.0. Procedencia: http://www.flickr.com/photos/chuchipi/6121091526/in/photostream/lightbox/ |
 |
Autoría: Jesús Pereira Iglesias. Licencia: CC BY-NC 2.0. Procedencia: http://www.flickr.com/photos/chuchipi/6121091426/in/photostream/lightbox/ |